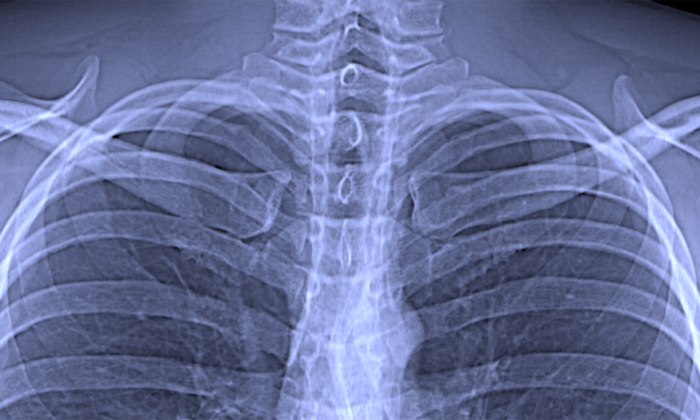
Dunkelfeld-Röntgen verbessert Diagnose von Lungenerkrankungen
Neue Röntgentechnologie im Patienteneinsatz

Millionenfach führen schwere Erkrankungen des Atmungssystems zu stark eingeschränkter Lebensqualität. Jedes Jahr sterben allein in Deutschland mehr als 100.000 Menschen an schweren Lungenerkrankungen. Typisch für eine lebensgefährliche chronisch obstruktive Lungenerkrankung (chronic obstructive pulmonary disease, COPD) sind teilweise zerstörte Lungenbläschen und eine Aufblähung der Lunge (Emphysem).
In normalen Röntgenaufnahmen sind die feinen Unterschiede im Gewebe jedoch kaum sichtbar. Detaillierte diagnostische Informationen liefern erst fortschrittliche medizinische Bildgebungstechnologien, bei denen im Computer viele Einzelbilder zusammengesetzt werden. Eine schnelle und kostengünstige Option mit geringer Strahlenbelastung für Früherkennung und Nachuntersuchungen fehlt bisher.
Diese Lücke könnte ein an der TU München entwickeltes Verfahren schließen: das Dunkelfeld-Röntgen. In der aktuellen Ausgabe von „Lancet Digital Health“ präsentiert ein Forschungsteam, angeführt von Franz Pfeiffer, Professor für biomedizinische Physik und Direktor des Munich Institute of Biomedical Engineering der TUM, nun Ergebnisse einer ersten klinischen Studie mit Patienten, bei der die neue Röntgen-Technologie zur Diagnose der Lungenkrankheit COPD eingesetzt wurde.
Der Wellencharakter des Röntgenlichts macht‘s möglich
Die konventionelle Röntgen-Bildgebung beruht auf der Abschwächung des Röntgenlichts auf seinem Weg durch das Gewebe. Die Dunkelfeld-Technologie dagegen nutzt Anteile des Röntgenlichts, die gestreut werden und beim konventionellen Röntgen unbeachtet bleiben.
Die neue Methode nutzt damit das physikalische Phänomen der Streuung auf ähnliche Weise wie die schon länger bekannte Dunkelfeldmikroskopie mit sichtbarem Licht: Diese macht es möglich, Strukturen weitgehend transparenter Objekte sichtbar zu machen. Im Mikroskop erscheinen sie als helle Strukturen vor einem dunklen Hintergrund, was der Methode ihren Namen verleiht.
„An Grenzflächen zwischen Luft und Gewebe ist diese Streuung beispielsweise besonders stark“, erklärt Pfeiffer. „Dadurch lassen sich in einem Dunkelfeldbild der Lunge Bereiche mit intakten, also luftgefüllten, Lungenbläschen klar von Regionen unterscheiden, in denen weniger intakte Lungenbläschen vorhanden sind.“

Geringere Strahlendosis
Eine Untersuchung mit der Dunkelfeld-Röntgen-Technik ist außerdem mit einer deutlich geringeren Strahlendosis verbunden als die heute verwendete Computertomografie. Denn sie erfordert nur eine einzelne Aufnahme pro Patientin oder Patient, während für die Computertomografie zahlreiche Einzelaufnahmen aus verschiedenen Richtungen erstellt werden müssen.
„Wir rechnen mit einer um den Faktor Fünfzig reduzierten Strahlenbelastung“, sagt Franz Pfeiffer. Darüber hinaus haben die ersten klinischen Ergebnisse bestätigt, dass das Dunkelfeld-Röntgen zusätzliche bildliche Informationen über die zugrundeliegende Mikrostruktur der Lunge liefert.
„Angesichts des engen Zusammenhangs zwischen der Alveolarstruktur und dem funktionellen Zustand der Lunge ist diese Fähigkeit für die Lungenheilkunde von großer Bedeutung,“ erklärt Dr. Alexander Fingerle, Oberarzt des Instituts für Diagnostische und Interventionelle Radiologie am Klinikum rechts der Isar der TUM. „Das Dunkelfeld-Röntgen könnte so zu einer besseren Früherkennung von COPD und anderen Lungenerkrankungen in Zukunft beitragen.“
Zukünftig bessere Röntgengeräte für die Früherkennung
Franz Pfeiffer hofft, mit diesen ersten klinischen Ergebnissen an Patienten die Durchführung weiterer klinischer Studien und die Entwicklung marktfähiger Geräte zu beschleunigen, die die Dunkelfeld-Methode nutzen.
„Mit der Dunkelfeld-Röntgen-Technologie haben wir aktuell eine Chance, die Früherkennung von Lungenkrankheiten deutlich zu verbessern und gleichzeitig auch breiter als bisher einzusetzen,“ betont Pfeiffer.
Da die Dunkelfeld-Bildgebung nicht auf COPD beschränkt ist, sind auch weitere translationale Studien zu anderen Lungenpathologien wie Fibrose, Pneumothorax, Lungenkrebs und Lungenentzündung, einschließlich COVID-19, von großem Interesse.
Konstantin Willer, Alexander Fingerle, Wolfgang Noichl, Fabio De Marco, Manuela Frank, Theresa Urban, Rafael Schick, Alex Gustschin, Bernhard Gleich, Julia Herzen, Thomas Koehler, Andre Yaroshenko, Thomas Pralow, Gregor Zimmermann, Bernhard Renger, Andreas Sauter, Daniela Pfeiffer, Marcus Makowski, Ernst Rummeny, Philippe Grenier, Franz Pfeiffer
X-ray dark-field chest imaging for detection and quantification of emphysema in patients with chronic obstructive pulmonary disease: a diagnostic accuracy study
Lancet Digital Health, Volume 3, ISSUE 11, e733-e744, November 01, 2021 – DOI: 10.1016/S2589-7500(21)00146-1
Die Arbeiten wurden unterstützt durch das European Research Council im Rahmen eines Advanced Grants und die Philips Medical Systems DMC GmbH. Mitautor Thomas Köhler (Philips) war Rudolf Diesel Industry Fellow des TUM Institute for Advanced Study (TUM-IAS), das aus Mitteln der Exzellenzinitiative des Bundes und der Länder sowie des Marie Curie COFUND-Programm der EU gefördert wird. Ein Teil der Arbeiten wurde in Kooperation mit der Karlsruhe Nano Micro Facility (KNMF), einer Helmholtz-Forschungsinfrastruktur am Karlsruher Institut für Technologie (KIT), durchgeführt.
Technische Universität München
Corporate Communications Center
- Dr. Andreas Battenberg
- battenberg@zv.tum.de
- presse@tum.de
- Teamwebsite
Kontakte zum Artikel:
Prof. Dr. Franz Pfeiffer
Lehrstuhl für Biomedizinische Physik
Department für Physik / Munich Institute of Biomedical Engineering (MIBE)
James-Franck-Str. 1, 85748 Garching
Tel.: +49 89 289 12551 (Büro) – +49 89 289 12552 (Sekretariat)
E-Mail: franz.pfeiffer@tum.de